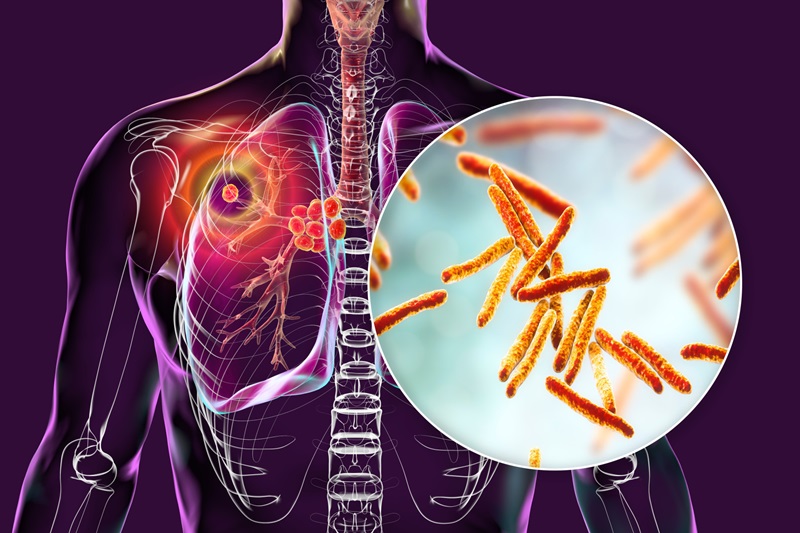
Comprender cómo la bacteria infecta, sobrevive y evade al sistema inmune es clave para desarrollar mejores tratamientos y mitigar los efectos de una enfermedad que sigue afectando a millones de personas en el mundo. Mycobacterium tuberculosis, la bacteria causante de la enfermedad fue identificada en 1882 y ya llevaba tres millones de años viviendo en la Tierra.
Se piensa que esta enfermedad es un problema del pasado, sin embargo, actualmente es la principal causa de muerte por un agente infeccioso a nivel mundial. Se estima que en 2024 esta patología ocasionó alrededor de 1,2 millones de muertes. En Argentina, los datos más recientes relevados en el boletín epidemiológico nacional indican que en 2025 se notificaron 15.599 nuevos infectados.
La bacteria tiene la capacidad de entrar, infectar y permanecer escondida en el huésped activando un estado de dormancia, en el cual se reproduce pero a tasas muy bajas, estableciendo una infección latente. Es decir, la persona está infectada pero no tiene síntomas y puede estarlo por muchos años sin enfermarse”, expresa Gabriela Gago, investigadora del CONICET en el Instituto de Biología Molecular y Celular de Rosario (IBR, CONICET-UNR) y presidenta de la Sociedad Latinoamericana de Tuberculosis y Otras Micobacteriosis (SLAMTB).

(Gabriela Gago en el laboratorio del IBR)
Se estima que un 25 por ciento de la población mundial tiene una infección latente de tuberculosis, y si bien existen algunos test para identificar estos casos, no es fácil: “El problema es que la tuberculosis estigmatiza mucho. Aunque sea una enfermedad infecciosa que cualquiera puede contagiarse, en general afecta a las poblaciones más vulnerables, a las poblaciones más pobres. Es un grave problema en las cárceles, en personas que viven en la calle o en residencias comunitarias. Si a alguien le identifican tuberculosis, muchas veces ni lo dice e incluso hay resistencia de los contactos directos a ser evaluados, porque da miedo y mucha gente prefiere no saber”, señala Gago.
Pero luego, cuando el sistema inmune de estas personas se deprime -por mal nutrición, un tratamiento oncológico, diabetes agudas u otras enfermedades inmunodepresoras como el HIV- la infección puede reactivarse, la bacteria se replica a tasas más altas, los síntomas aparecen y pueden causar la muerte por insuficiencia respiratoria si no se trata a tiempo.
El esquema terapéutico dura seis meses y requiere la administración combinada de cuatro antibióticos diferentes. En consecuencia, “es alto el porcentaje de gente que abandona o no le da continuidad al tratamiento, y eso supone recaídas y un problema enorme en términos de la generación de resistencias a los antibióticos; esto no solo complica al paciente, sino que también es un peligro para toda la comunidad”, advierte Luciana Balboa, investigadora del consejo que estudia la inmunología de la tuberculosis en el Instituto de Investigaciones Biomédicas en Retrovirus y Sida de la Facultad de Ciencias Médicas (INBIRS, CONICET-UBA). Por ello, señala, es importante generar innovaciones terapéuticas que puedan acortar los tratamientos y evitar la aparición de resistencias a los antibióticos.
En esa búsqueda se encuentran Gago y su equipo especializado en microbiología. Poniendo el foco sobre M. tuberculosis, estudian cómo el metabolismo de la bacteria determina la compleja y dinámica estructura de su envoltura celular. “Tiene varias capas, una es como la membrana que tienen todas las células, pero además en esta bacteria hay otras capas que la rodean y que tienen moléculas (especialmente los lípidos) que sabemos están relacionados con su virulencia”, explica Gago. Se ha comprobado que, dependiendo de las moléculas lipídicas que la bacteria fabrique y presente en esta envoltura, se establece la comunicación con el huésped y determina si desata una infección activa o si permanece en estado de latencia. “Siempre nos interesó entender cómo se fabrican esos lípidos, a qué señales responden y cómo se modula la composición de la envoltura para poder intervenir en esa definición y hacer que las bacterias sean más vulnerables”. Manipulando genéticamente las bacterias en el laboratorio, buscan identificar moléculas reguladoras de la síntesis de lípidos, que sirvan como anti-virulentos, es decir que resulten esenciales para la virulencia de la bacteria, pero no para su vida.
Por su parte, las investigaciones de Balboa se centran en la respuesta inmunológica y cómo M. tuberculosis puede manipularla para evadir las defensas del huésped. Una característica determinante de este patógeno es que puede alojarse dentro de los macrófagos, que son células del sistema inmunitario que “vigilan” y recorren los tejidos en busca de patógenos y desperdicios a los cuales fagocitan (ingieren) para eliminarlos. “Entonces estas células tienen un rol dual en la vida de la micobacteria; la misma célula que por un lado le da alojamiento y le permite sobrevivir es la misma que debería matarla. Hay un fino balance entre cuán buenos son nuestros macrófagos en desplegar mecanismos que le permitan eliminar a la bacteria versus todos los mecanismos de patogenicidad que despliega el microorganismo, ahí se define quién gana y qué pasa”, señala Balboa. Analizando muestras de pacientes con tuberculosis, ella y su equipo identificaron la abundancia de ciertos lípidos que inhiben la capacidad microbicida de los macrófagos, o sea su capacidad de matar bacterias. Estas moléculas lipídicas son fabricadas por el huésped, pero inducidas en el marco de la infección tuberculosa. Según Balboa, modulando farmacológicamente la síntesis de esos lípidos, podrían hacer que los macrófagos recuperen su capacidad de eliminar a la bacteria. “Estamos evaluando una droga que actualmente se utiliza para tratar el asma y que podría inhibir la síntesis de las enzimas involucradas en la producción de estos lípidos. La idea sería usar esta droga como complemento para mejorar la respuesta inmunológica del organismo y de ese modo acortar el tratamiento con antibióticos”.
Las investigadoras llevan más de 20 años dedicados al estudio de esta enfermedad, para Gago trabajar con este microorganismo es apasionante porque en este patógeno todo es diferente, todo es más complejo: “Me encantaría poder hablar un día con la bacteria y preguntarle por qué toma algunas decisiones que son tan difíciles de entender desde la biología”, reflexiona.
Según Balboa si se le quiere poner fin, hay que visibilizar el problema y enfrentarlo desde múltiples ángulos: “Se necesita inversión, compromiso político y estrategias interdisciplinarias”. (fuente: CONICET)

(Luciana Balboa en su laboratorio del INBIRS)